フィコンパに係る医薬品リスク管理計画書(RMP)
フィコンパ点滴静注用2mg
- くすりのしおり
- 日本語版 くすりのしおりご使用にあたって
最新のお知らせ
-
2021.2.26
- 医薬品リスク管理計画
- 脳神経・精神
- フィコンパ
フィコンパに係る医薬品リスク管理計画書(RMP)
-
2020.1.23
- 安全性・適正使用
- 脳神経・精神
- フィコンパ
フィコンパ錠2mg/錠4mg/細粒1% 添付文書改訂のお知らせ
副作用情報に該当するお知らせはありません
製品情報に該当するお知らせはありません
その他に該当するお知らせはありません
製品概要
※ご使用にあたっては電子添文をご確認ください。
※文頭に「**」が記載されている箇所が最新の改訂内容です。
指導箋
片頭痛に関する指導箋
適正使用に関する基本情報
関連コンテンツ
-
epiサポ 2
てんかんを持つひとと、そのご家族が、安心して暮らすためのアドバイスをご紹介します。
-

ダウンロード コンテンツ
てんかん診療・講演会でお使いいただける動画・PPT・PDFをダウンロードできます
-
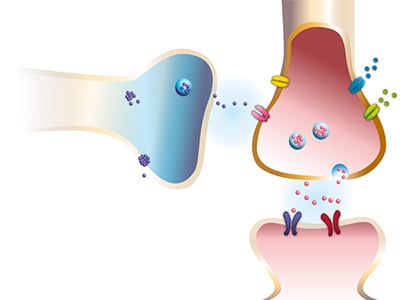
てんかんとAMPA受容体との 関わりについて
-
複雑部分発作(焦点意識減損発作)
発作中の意識は失われていたり途切れたりしている。一点をじっと凝視するような状態や、口をクチュクチュと動かしたり、手をもぞもぞ動かすような症状が見られる。
-
単純部分発作(焦点意識保持発作)
発作中の意識は保たれている。あるはずのない光や物が見えたり、不安や恐怖感に襲われることもあれば、こみ上げる胃部不快感などの症状が見られる。 複雑部分発作(焦点意識減損
-

さまざまな種類の発作があります。そして、同じ患者様では、同じてんかん症状が現れます。


